Химия | 10 - 11 классы
СРОЧНО (см.
В вложения)
Какое количество теплоты (кДж) выделяется при образовании 1 моль оксида мышьяка(5) по уравнению реакции
3As2O3(к) + 2O3() = 3As2O5(к) + 1096, 3 кДж.

Если энтальпия образования SO3 равна – 297 кДж / моль, тогда количество теплоты, выделяемое при сгорании равно…?
Если энтальпия образования SO3 равна – 297 кДж / моль, тогда количество теплоты, выделяемое при сгорании равно….
1) 297 кДж 2) 594 кДж 3) 148, 5 кДж 4) 74, 25 кДж.

Вычислите теплоту перехода графита в алмаз, если при образовании 1 моль СO2 из графита выделяется - 393, 5 кДж / моль, а из алмаза выделяется - 395, 4 кДж / моль?
Вычислите теплоту перехода графита в алмаз, если при образовании 1 моль СO2 из графита выделяется - 393, 5 кДж / моль, а из алмаза выделяется - 395, 4 кДж / моль.
Очень нужно!
Плиз!

Какое количество теплоты выделяется при сгорании 2 моль фосфора по уравнению реакции 4P 5 O2 = 2 P2 O5 3010 кДж?
Какое количество теплоты выделяется при сгорании 2 моль фосфора по уравнению реакции 4P 5 O2 = 2 P2 O5 3010 кДж.

Теплота образования хлороводорода из простых веществ равна 92 кДж / моль?
Теплота образования хлороводорода из простых веществ равна 92 кДж / моль.
Количество теплоты, выделившееся при образовании 146 г хлороводорода, равно
1) 92 кДж 2) 184 кДж 3) 18, 4 кДж 4) 368 кДж.

При образовании из простых веществ 1 моль оксида серы(IV) выделяется теплота в количестве 332, 8 кДж?
При образовании из простых веществ 1 моль оксида серы(IV) выделяется теплота в количестве 332, 8 кДж.
Сколько выделится теплоты при сгорании 1 г серы?

Для образования 1 моля NO требуется 90, 37 кДж теплоты?
Для образования 1 моля NO требуется 90, 37 кДж теплоты.
Вычислите массу оксида азота (II), образовавшегося при поглощении теплоты в количестве 9037 кДж.

Для образования одногоо моля NO требуется 90, 37 кДж теплоты?
Для образования одногоо моля NO требуется 90, 37 кДж теплоты.
Вычислите массу оксида азота (2валентность), при поглощении теплоты в количестве 9037 кДж.
Решение в два действия.

Какое количество теплоты (кДж) выделяется при образовании 1 моль оксида мышьяка (V) по уравнению реакции 3 As2O3(к) + 2 O3(г) = 3 As2O5(к) + 1096, 3 кДж?
Какое количество теплоты (кДж) выделяется при образовании 1 моль оксида мышьяка (V) по уравнению реакции 3 As2O3(к) + 2 O3(г) = 3 As2O5(к) + 1096, 3 кДж.

Для образования 1 моля NO требуется 90?
Для образования 1 моля NO требуется 90.
37 кдж теплоты.
Вычислите массу оксида азота(2) , образовавшегося при поглощении теплоты в количестве 9037 кдж.

В соответствии с термохимическим уравнением 2so2 + o2 = 2so3 + 196, 6 кдж, вычеслити какое количество теплоты (кдж) выделяется при образовании 60 г оксида серы (vl) (SO3)?
В соответствии с термохимическим уравнением 2so2 + o2 = 2so3 + 196, 6 кдж, вычеслити какое количество теплоты (кдж) выделяется при образовании 60 г оксида серы (vl) (SO3).
На этой странице находится вопрос СРОЧНО (см?. Здесь же – ответы на него, и похожие вопросы в категории Химия, которые можно найти с помощью простой в использовании поисковой системы. Уровень сложности вопроса соответствует уровню подготовки учащихся 10 - 11 классов. В комментариях, оставленных ниже, ознакомьтесь с вариантами ответов посетителей страницы. С ними можно обсудить тему вопроса в режиме on-line. Если ни один из предложенных ответов не устраивает, сформулируйте новый вопрос в поисковой строке, расположенной вверху, и нажмите кнопку.

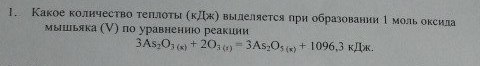


Решаем через пропорцию
3моль соответствует - 1096, 3
1моль соответствует - х(т.
Е. неизвестное кол - во теплоты)
3 - - - - - - - - - 1096, 3
1 - - - - - - - - - х
х = 1096, 3 делим на 3
х = 365, 4
Ответ : 365, 4 Кдж теплоты выделяется))).