
Химическое равновесие сместится в сторону продуктов реакции при 2SO2 + O2 = 2SO3 + Q понижении температуры повышении температуры добавлении катализатора уменьшения давления?
Химическое равновесие сместится в сторону продуктов реакции при 2SO2 + O2 = 2SO3 + Q понижении температуры повышении температуры добавлении катализатора уменьшения давления.

В реакции СO(г) + 2Н2(г) ⇄ СН3ОН(г) + Q равновесие сместится в сторону продуктов реакции при 1) повышении температуры и повышении давления 2) повышении температуры и понижении давления 3) понижении те?
В реакции СO(г) + 2Н2(г) ⇄ СН3ОН(г) + Q равновесие сместится в сторону продуктов реакции при 1) повышении температуры и повышении давления 2) повышении температуры и понижении давления 3) понижении температуры и повышении давления
4) понижении температуры и понижении давления
Думаю 2, правильно?

Увеличению выхода метилового спирта в ходе реакцииCO(г) + 2H2(г) = CH3OH(г) + Qспособствует1) понижение давления и повышение температуры2) повышение температуры и использование катализатора3) повышени?
Увеличению выхода метилового спирта в ходе реакции
CO(г) + 2H2(г) = CH3OH(г) + Q
способствует
1) понижение давления и повышение температуры
2) повышение температуры и использование катализатора
3) повышение давления и понижение температуры
4) понижение давления и использование катализатора.

Как изменится скорость реакции 2СО + О2 = 2СО2 при повышении давления?
Как изменится скорость реакции 2СО + О2 = 2СО2 при повышении давления?
При понежениии давления?

Почему при повышении температуры растворимость газов уменьшается, а при повышении давления увеличивается?
Почему при повышении температуры растворимость газов уменьшается, а при повышении давления увеличивается?

Химическое равновесие в системе CO2 + C - 2CO - 173 кДж смещается в сторону продукта реакции при 1) повышении давления 2)повышение температуры 3)понижение температуры 4)использование катализатора?
Химическое равновесие в системе CO2 + C - 2CO - 173 кДж смещается в сторону продукта реакции при 1) повышении давления 2)повышение температуры 3)понижение температуры 4)использование катализатора.

Химическое равновесие в системе CO2 + C - 2CO + 173 кДж смещается в сторону продукта реакции при 1) повышении давления 2)повышение температуры 3)понижение давления 4)использование катализатора?
Химическое равновесие в системе CO2 + C - 2CO + 173 кДж смещается в сторону продукта реакции при 1) повышении давления 2)повышение температуры 3)понижение давления 4)использование катализатора.

В какой реакции повышение давления в системе приведет к повышению выхода продуктов реакции и почему?
В какой реакции повышение давления в системе приведет к повышению выхода продуктов реакции и почему?
1)2H2O = 2H2 + O2 + Q 2)N2 + 3H3 = 2NH3 + Q 3)I2 + H2 = 2HI - Q 4)N2 + O2 = 2NO - Q.

В какой реакции повышение давления в системе приведет к повышению выхода продуктов реакции и почему?
В какой реакции повышение давления в системе приведет к повышению выхода продуктов реакции и почему?

В каком направлении смещается равновесие в системе 2CO(Г) + O2(Г) = 2CO2 (Г), H < ; 0 : а) при увеличении давления ; б) при понижении температуры ; в) при пропускании кислорода через реактор?
В каком направлении смещается равновесие в системе 2CO(Г) + O2(Г) = 2CO2 (Г), H < ; 0 : а) при увеличении давления ; б) при понижении температуры ; в) при пропускании кислорода через реактор?
Предложите условия повышения выхода продуктов реакции.
На этой странице находится ответ на вопрос При повышении давления выход продукта уменьшается в реакциях ?, из категории Химия, соответствующий программе для 1 - 4 классов. Чтобы посмотреть другие ответы воспользуйтесь «умным поиском»: с помощью ключевых слов подберите похожие вопросы и ответы в категории Химия. Ответ, полностью соответствующий критериям вашего поиска, можно найти с помощью простого интерфейса: нажмите кнопку вверху страницы и сформулируйте вопрос иначе. Обратите внимание на варианты ответов других пользователей, которые можно не только просмотреть, но и прокомментировать.

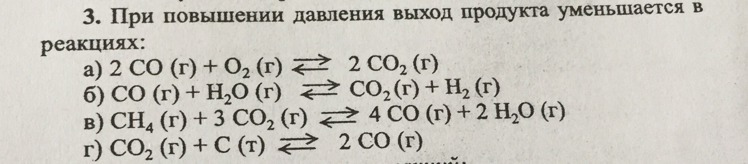



В, г.