Химия | 10 - 11 классы
Составьте электронный баланс, закончите уравнение, укажите процессы окисления и восстановления.

Задание 10 : номер 1, 2, 3 : Используя метод электронного баланса подберите коэффициенты в уравнении реакции и определите какой из процессов является окислением какой восстановлению Укажите окислитель?
Задание 10 : номер 1, 2, 3 : Используя метод электронного баланса подберите коэффициенты в уравнении реакции и определите какой из процессов является окислением какой восстановлению Укажите окислитель и восстановитель.

H2O2 + KMnO4 + H2SO4 → O2 + MnSO4 + K2SO4 + …реакция?
H2O2 + KMnO4 + H2SO4 → O2 + MnSO4 + K2SO4 + …
реакция.
Допишите недостающий продукт вместо многоточия.
Составьте уравнения электронного баланса, уравняйте приведённую реакцию, дайте названия процессам и реагентам (укажите процессы окисления и восстановления, окислитель и восстановитель).

6. Расставьте коэффициенты в схемах уравнений реакций с помощью электронного баланса, укажите окислитель, восстановитель, процесс окисления, восстановления, покажите переход электронов?
6. Расставьте коэффициенты в схемах уравнений реакций с помощью электронного баланса, укажите окислитель, восстановитель, процесс окисления, восстановления, покажите переход электронов.
А) К + N2 = К3N
Б) ZnS + O2 = ZnO + SO2.

Для уравнения 2Zn + O2 = 2Zn0 составьте схему электронного баланса, укажите окислитель и восстановитель, процессы окисления и восстановления?
Для уравнения 2Zn + O2 = 2Zn0 составьте схему электронного баланса, укажите окислитель и восстановитель, процессы окисления и восстановления.

Закончить уравнение реакции, составить электронный баланс, указать процессы окисления и восстановления :MnO2 + HCL - > MnCl2 + Cl2 + ?
Закончить уравнение реакции, составить электронный баланс, указать процессы окисления и восстановления :
MnO2 + HCL - > MnCl2 + Cl2 + ?

Запишите реакции взаимодействия меди с разбавленной и концентрированной азотной кислотой?
Запишите реакции взаимодействия меди с разбавленной и концентрированной азотной кислотой.
Расставьте коэффициенты методом электронного баланса.
Укажите процесс окисления, процесс восстановления, окислитель, восстановитель.

Расставьте коэффициенты в схемах уравнений реакций с помощью электронного баланса, укажите окислитель, восстановитель, процесс окисления, восстановления, покажите переход электронов?
Расставьте коэффициенты в схемах уравнений реакций с помощью электронного баланса, укажите окислитель, восстановитель, процесс окисления, восстановления, покажите переход электронов.
А) H2 + Br2 = HBr Б)CrO3 + H2 = Cr + H2O.

CO + Fe2O3 = FeO + CO2 УКАЖИТЕ окислитель восстановитель процессы окисления и восстановления , составьте электронный баланс определите коэфиценты?
CO + Fe2O3 = FeO + CO2 УКАЖИТЕ окислитель восстановитель процессы окисления и восстановления , составьте электронный баланс определите коэфиценты.

В уравнении окислительно - восстановительной реакции Са + Н2SO4(к)→СaSO4 + H2S + H2O расставьте коэфиценты методом электрон?
В уравнении окислительно - восстановительной реакции Са + Н2SO4(к)→СaSO4 + H2S + H2O расставьте коэфиценты методом электрон.
Баланса, укажите процессы окисления и восстановления, окислитель и восстановитель.

Расставьте коэффициенты методом электронного баланса?
Расставьте коэффициенты методом электронного баланса.
Укажите окислитель и восстановитель, процессы окисления и восстановления : KMnO4 + H2O + Na2SO3 = MnO2(т) + Na2SO4 + KOH.
Перед вами страница с вопросом Составьте электронный баланс, закончите уравнение, укажите процессы окисления и восстановления?, который относится к категории Химия. Уровень сложности соответствует учебной программе для учащихся 10 - 11 классов. Здесь вы найдете не только правильный ответ, но и сможете ознакомиться с вариантами пользователей, а также обсудить тему и выбрать подходящую версию. Если среди найденных ответов не окажется варианта, полностью раскрывающего тему, воспользуйтесь «умным поиском», который откроет все похожие ответы, или создайте собственный вопрос, нажав кнопку в верхней части страницы.

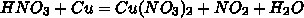




4HNO₃ + Cu = Cu(NO₃)₂ + 2NO₂ + 2H₂O
N⁺⁵ + 1e = N⁺⁴ 2 азот окислитель, процесс восстановления
Cu⁰ - 2e = Cu⁺² 1 медь восстановитель, процесс окисления.