
Хлорид железа 2 можно получить взаимодействием веществ, формулы которых : а) FeSO4 и KCl б) Fe(OH)2 и NaCl в) FeO и KCl г) Fe(OH)2 и HCl?
Хлорид железа 2 можно получить взаимодействием веществ, формулы которых : а) FeSO4 и KCl б) Fe(OH)2 и NaCl в) FeO и KCl г) Fe(OH)2 и HCl.

Ребята, помогите, почему у FeO?
Ребята, помогите, почему у FeO.
У железа степень окисления 2?
Напишите решение того, как вы нашли О.
С? .

Найдите медь и железу : a) Cu2O ; CuO?
Найдите медь и железу : a) Cu2O ; CuO.
Б) FeO ; Fe2O3.
Пжж срочно 8 класс.

Сколько грамм железа нужно взять для получения 112 гр?
Сколько грамм железа нужно взять для получения 112 гр.
FeO.

FeO + HNO3Помогите пожалуйста?
FeO + HNO3
Помогите пожалуйста.

Максимальным является содержание железа в соединении :1)CuFeS22)Fes23)Fe2O34)FeO(цифры везде маленькие)?
Максимальным является содержание железа в соединении :
1)CuFeS2
2)Fes2
3)Fe2O3
4)FeO
(цифры везде маленькие).

Определите степени окисления атомов элементов и укажите какая из реакций, схемы которых приведены ниже, является окислительно - восстановительной?
Определите степени окисления атомов элементов и укажите какая из реакций, схемы которых приведены ниже, является окислительно - восстановительной.
А)FeO + HCL→FeCL2 + H2O б)FeO + CO→Fe + CO2.

Определите вид химических элементов FeO, Br2?
Определите вид химических элементов FeO, Br2.

HNO3 + FeO РИО хелп плиз?
HNO3 + FeO РИО хелп плиз.

Какое соединениебогаче железом FeO или Fe2O3?
Какое соединениебогаче железом FeO или Fe2O3.
Вы перешли к вопросу Определить вещество белее богато железом FeO, Fe2O3?. Он относится к категории Химия, для 5 - 9 классов. Здесь размещен ответ по заданным параметрам. Если этот вариант ответа не полностью вас удовлетворяет, то с помощью автоматического умного поиска можно найти другие вопросы по этой же теме, в категории Химия. В случае если ответы на похожие вопросы не раскрывают в полном объеме необходимую информацию, то воспользуйтесь кнопкой в верхней части сайта и сформулируйте свой вопрос иначе. Также на этой странице вы сможете ознакомиться с вариантами ответов пользователей.

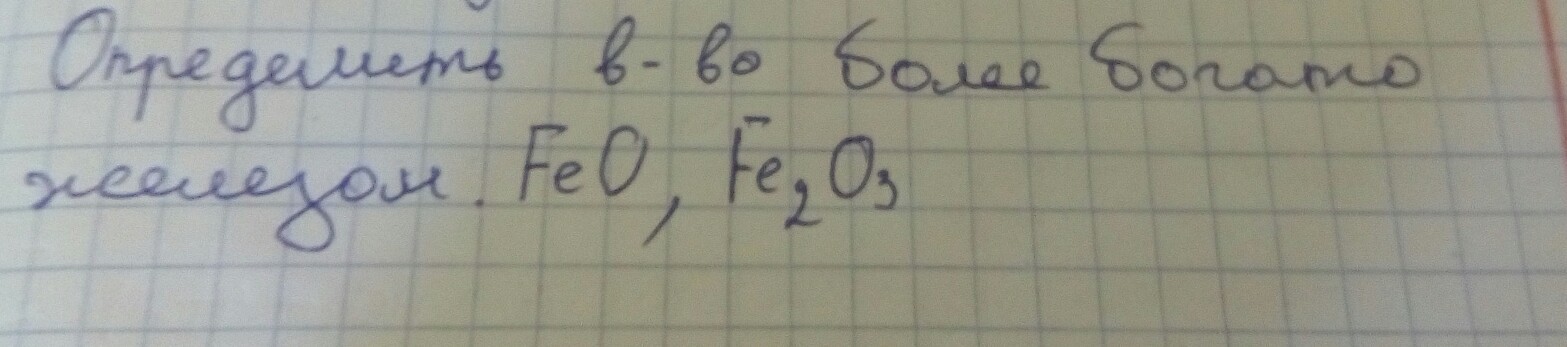


Первое.
Это можно даказать с помощю пропорции.
1)1 / 1 2)2 / 3.
1 / 1>2 / 3
1>0.
6.