
Помогите решить окислительно - восстановительные реакции?
Помогите решить окислительно - восстановительные реакции.

Окислительно - восстановительные реакции S + NO2 = SO2 + N2?
Окислительно - восстановительные реакции S + NO2 = SO2 + N2.

Помогите, пожалуйста, с заданиями по химии?
Помогите, пожалуйста, с заданиями по химии!
Окислительно - восстановительная реакция.

Составьте окислительно - восстановительную реакцию?
Составьте окислительно - восстановительную реакцию.

Разберите уравнение реакции как окислительно восстановительное NO2 + CO = CO2 + N2?
Разберите уравнение реакции как окислительно восстановительное NO2 + CO = CO2 + N2.

Укажите, какие из реакций являются окислительно восстановительными?
Укажите, какие из реакций являются окислительно восстановительными.

Приведите уравнения хим?
Приведите уравнения хим.
Реакций серы и составьте для них окислительно - восстановительные реакции.
Заранее, спасибо!

Охарактеризуйте реакцию промышленного получения аммиака по всем признакам :обратимаянеобратимаяокислительно - восстановительнаяне окислительно - восстановительнаякаталитическаянекаталитическаяреакция ?
Охарактеризуйте реакцию промышленного получения аммиака по всем признакам :
обратимая
необратимая
окислительно - восстановительная
не окислительно - восстановительная
каталитическая
некаталитическая
реакция соединения
реакция замещения
реакция обмена
реакция разложения
экзотермическая
эндотермическая.

Окислительно восстановительными являются реакции?
Окислительно восстановительными являются реакции.

Составить окислительно - восстановительные реакции : 2H2 + O2 = 2H2O?
Составить окислительно - восстановительные реакции : 2H2 + O2 = 2H2O.
На этой странице находится вопрос Напишите окислительно - восстановительные реакции?. Здесь же – ответы на него, и похожие вопросы в категории Химия, которые можно найти с помощью простой в использовании поисковой системы. Уровень сложности вопроса соответствует уровню подготовки учащихся 5 - 9 классов. В комментариях, оставленных ниже, ознакомьтесь с вариантами ответов посетителей страницы. С ними можно обсудить тему вопроса в режиме on-line. Если ни один из предложенных ответов не устраивает, сформулируйте новый вопрос в поисковой строке, расположенной вверху, и нажмите кнопку.

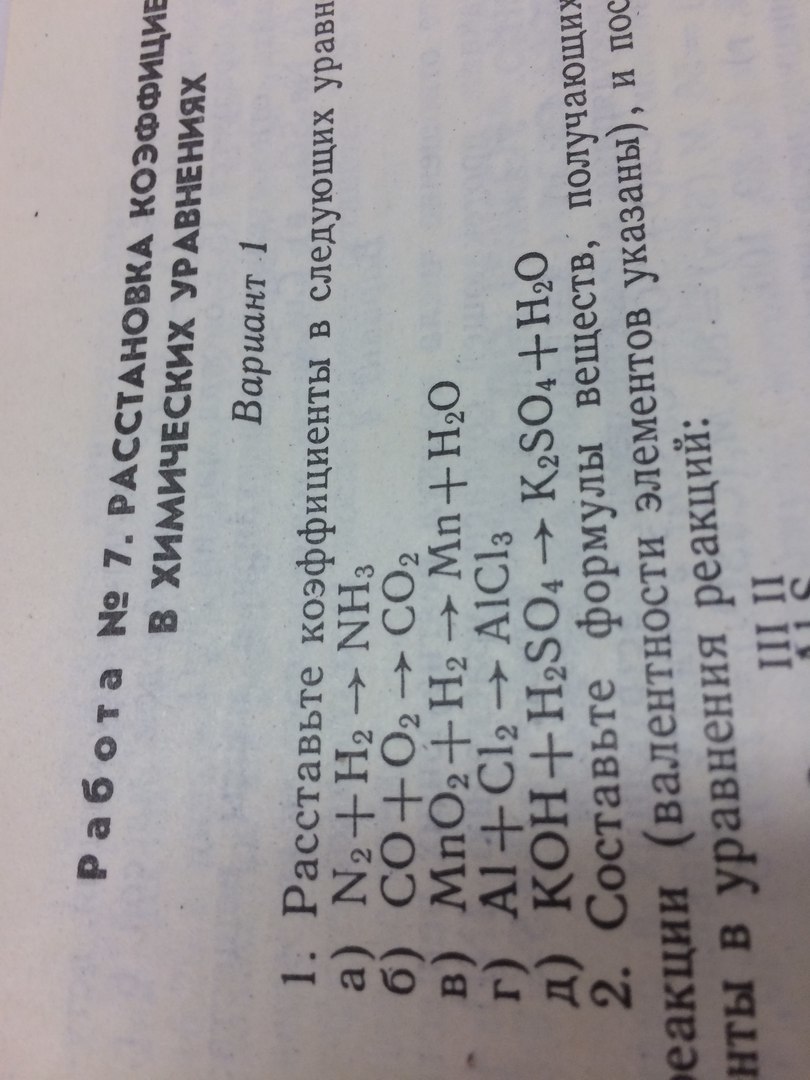



1. а)N2(0) + H2(0) = N( - 3)H( + )3N2(0) + 6e = 2N( - 3)|1 окислитель, в - еH2(0) - 2e = 2H( + ) |3 восстановитель, ок - еN2 + 3H2 = 2NH3
б)С ( + 2) - 2ē = > С ( + 4) | 2 | восстановитель, окисление
2О (0) + 4ē = > 2O ( - 2) | 1| окислитель, восстановление
2CO + O2 = 2CO2
в) + 4 - 2 0 + 2 - 2 + 1 - 2
MnO2 + H2 = MnO + H2O
1| H2[0] - 2e = 2H[ + 1] | 1 восстановитель, окисление
1|Mn[ + 4] + 2e = Mn[ + 2] | 1 окислитель, восстановление
г)Al - 3e = Al + 3 |2 восстановитель, окисление
Cl2 + 2e = 2Cl - |3 окислитель, восстановление
2Al + 3Cl2 = 2AlCl3
д)2КОН + Н2SO4 = К2SO4 + 2Н2ОТут не чего не изменяется, просто подбираем
Если помог, нажми кнопку Спасибо)).